专家信息:
钟涛,华东师范大学特聘教授,杰出青年基金获得者,重大科学研究计划首席科学家。钟涛教授于1987年毕业于复旦大学医学院(原上海医科大学)药物化学专业,获得理学学位;1995年在美国纽约州立大学的纽约冷泉港研究所获得联合遗传学博士;1995-2000年在美国哈佛大学医学院的心血管研究中心从事博士后研究;2001-2010年在美国范德堡(Vanderbilt)大学医学院先后担任医学系助理教授、副教授;2011年至2017年任复旦大学生命科学学院特聘教授。2017年至今任华东师范大学特聘教授;美国范德堡(Vanderbilt)大学医学院兼职教授。
教育及工作经历:
1982年9月-1987年6月,复旦大学医学院(原上海医科大学)药物化学专业,获学士学位。
1987年7月-1989年12月:复旦大学医学院(原上海医科大学) 硕士。
1995年7月-2000年8月,在美国麻省理工学院和哈佛医学院心血管研究中心任博士后研究员。
2002年,任美国范得堡 (Vanderbilt) 大学医学院药理系和发育细胞生物系助理教授,医学系副教授,复旦大学讲座教授。
2011年至2017年,复旦大学生命科学学院特聘教授,遗传工程国家重点实验室副主任。
2017年至今任华东师范大学特聘教授;美国范德堡(Vanderbilt)大学医学院兼职教授。
学术兼职及社会任职:
担任多个国际学术杂志的评审专家,包括Current Biology; Development; Developmental Biology; Circulation; Chemistry & Biology。
1、国家基金会评审委员会专家。
2、科技部中期评审委员会专家。
3、美国国立卫生研究院(NIH)项目评审委员会专家。
4、美国心脏学会(AHA)项目评审委员会专家。
5、美国遗传学学会会员, 发育生物学学会会员, 心脏协会会员。
主讲课程:
秋季学期开授专业选修课《发育与疾病》。
培养研究生情况:
资料更新中……
研究方向:
长远目标是阐明调控心血管发育和器官形成的细胞分子机制。心血管系统的动态性和复杂性使它成为既具有挑战性又吸引人的研究对象。发育和生长失控是人类心血管疾病的主要特点。我们主要以斑马鱼和小鼠为模式动物,利用遗传学、发育生物学和分子生物学的方法研究心脏和血管的分化形成和再生以及环境对心血管发育的影响。通过小分子化合物筛选来发现调控心血管发育和再生的信号传导网络和相应的药物前体。希望我们的研究不仅有助于解密人类心血管和其他疾病的细胞分子病因,并可能为细胞再生和组织自我修复的前沿疗法开辟广阔的思路。
研究成果和方向
1)利用基因编辑工具CRISPR/Cas9构建转基因、突变体斑马鱼以及开发更高效的单碱基编辑工具。
细胞谱系示踪是一种研究器官发育、组织损伤以及单细胞分化命运的重要手段,诱导性重组酶Cre/Loxp系统的应用为细胞谱系示踪技术打开了突破口。我们团队应用CRISPR/Cas9基因编辑工具(见图1)将外源性荧光报告基团序列或CreERT2序列定点整合到目的基因下游:①通过在斑马鱼活体中实时观察荧光基团表达位置及强度,可以反映目的基因内源性表达位置及表达丰度,以追踪表达此基因的细胞谱系;②通过控制外源诱导剂的时间窗口,诱导组织特异性表达的CreERT2对Loxp序列进行切割,以实现基因条件性敲除。同时,我们团队利用优化的高效单碱基编辑工具在斑马鱼当中进行基因编辑,构建斑马鱼疾病模型以模拟人类由于单碱基突变导致的疾病,为探索和研究人类单碱基突变疾病的病理机制及治疗方法奠定基础。基因碱基编辑器主要包括腺嘌呤碱基编辑器(ABE)与胞嘧啶碱基编辑器(CBE),可以在不产生DNA 双链断裂的情况下,在编辑窗口之内分别实现A:T>G:C 或者C:G>T:A 的转换,是基因编辑领域的颠覆性技术。我们团队合作开发了具有超高活性的腺嘌呤单碱基编辑器(hyABE),极大地提高了靠近PAM区A-to-G的转换效率,扩大了编辑窗口;研发的超高活性嘌呤嘧啶双碱基编辑器(eA&C-BEs和hyA&C-BEs)大幅提高了A-to-G和C-to-T(A/C)同时的编辑效率。研究证明hyABE在斑马鱼胚胎中可以有效催化A-to-G转换,编辑效率高达60%。hyABE能够在F0胚胎中引入纯合rps14E12G致病点突变,显著降低血红蛋白和红细胞数目,与人类血细胞发育异常(MDS)疾病表型一致,展现了hyABE在构建点突变疾病模型中的优势。同时,双碱基编辑器eA&C-BEs和hyA&C-BEs在斑马鱼胚胎中展现出较高的A-to-G和C-to-T同时转换效率。这些碱基编辑器的应用并没有引起斑马鱼胚胎发育致畸表型,提供了潜在的基因治疗新策略 (Nature Communications 2023) (https://www.ecnu.edu.cn/info/1094/62291.htm)。

图1.CRISPR/Cas9基本结构示意图
2)细胞纤毛与胚胎及心脏生长发育机制研究
我们发现前列腺素信号通路调控细胞纤毛生长和心脏不对称发育 (Nature Cell Biology, 2014;封面长文)。研究团队以斑马鱼和人类细胞为模型,通过分析Leakytail (Lkt) 遗传突变体,发现前列腺素转运蛋白缺失造成心脏与其他内脏器官随机性偏侧等异常表型。证明这些异常表型主要是由于胚胎发育时期细胞表面纤毛生长缺陷所引起。研究小组进一步发现LKT转运蛋白能够从细胞内转运前列腺素到细胞外,后者通过结合定位于纤毛膜上的G蛋白偶联受体,进而影响纤毛内转运蛋白 (IFT) 的正向速度,最终调节纤毛生长和心脏及其他内脏器官不对称发育(见图2)。此发现不仅揭示了在胚胎形成和器官发育中前列腺素信号的重要性,而且有助于解密人类纤毛运动综合症和先天性心脏病的细胞分子病因。《自然·细胞生物学》发表专题评论,认为“这项研究工作是前列腺素生理信号在发育领域的一个意想不到的重大发现”。
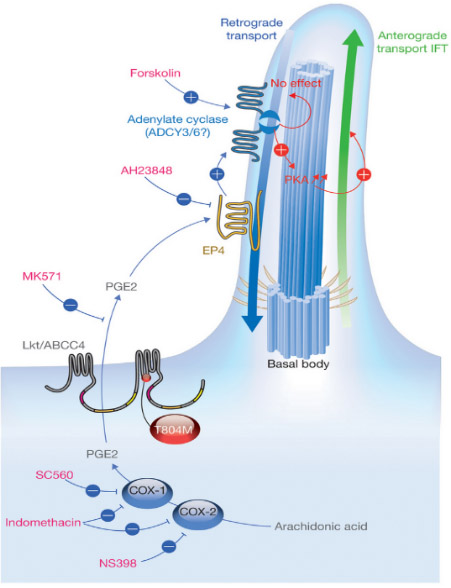
图2.PGE2信号通路调控纤毛生长
3)探索心脏发育及再生机制
成年哺乳动物心脏受损后再生能力有限,受损后心肌细胞被纤维疤痕取代,最终导致心力衰竭。与哺乳动物心脏不同,斑马鱼心脏损伤后可以通过心肌细胞去分化和增殖实现心脏再生;新生小鼠在出生一周内,损伤的心脏也可以通过心肌去分化和增殖完成再生。哺乳动物心脏再生能力有限,主要是由于细胞内在再生屏障与分子阻滞因子的存在,内源性再生障碍和负调控因子会阻碍心脏受损后心肌细胞去分化和增殖。探究这些再生过程中机制将为人类心脏疾病治疗提供新的启示。
我们实验室主要应用斑马鱼和小鼠作为心脏再生研究模型(见图3)。通过构建心肌特异性过表达T-box家族的转录因子(tbx20)品系,我们发现心肌细胞特异性过表达tbx20可以诱导受损区心肌细胞去分化,激活心内膜细胞BMP信号通路,促进受损心肌和心内膜再生(Frontiers in Cell and Developmental Biology 2020)。同时,我们揭示了bHLH转录因子Gridlock(Grl)/Hey2在心脏再生中的分子屏障机制;心肌细胞中条件性诱导Grl表达能够抑制受损后心肌细胞去分化与增殖;反之,Grl突变减少纤维化疤痕和促进心肌细胞增殖,增强心脏再生。研究表明心脏损伤诱导Grl表达下降,引起甲基转移酶Smyd2表达升高,进而调节Stat3甲基化和磷酸化,促进受损心肌去分化和再生(Development 2020)。
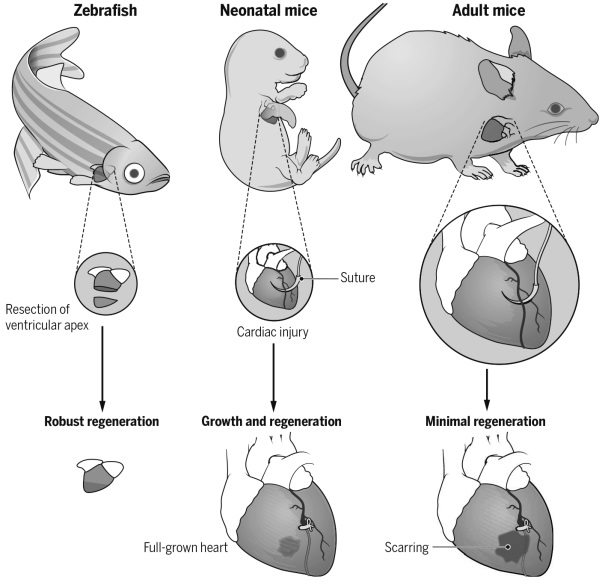
图3.心脏再生研究中常用的模式动物
4)研究造血干细胞增殖和分化的分子及细胞机制
造血干细胞(Hematopoietic and progenitor cells, HSPCs)是一群具有增殖、分化和重建能力的异质性干祖细胞。在血液形成过程中,造血干细胞是从主动脉-性腺-中肾区(Aorta-Gonad-Mesoneph, AGM)动脉腹侧生血内皮中产生,随后迁移至哺乳动物的胎肝(Feter Liver)或斑马鱼的尾部造血组织(Caudal Hematopoietic Tissue)进行快速增殖和分化,最终定植于骨髓或肾脏,维持成体造血(见图4)。我们研究团队以斑马鱼和小鼠为模式生物,结合人类造血干细胞,应用发育生物学、表观遗传学及基因组学方法,阐明了ATF7IP/SETDB1介导的组蛋白甲基化修饰是协调HSPC干细胞状态与多种血液谱系分化的一个关键检验点(Checkpoint),用于维持红系、髓系和淋巴系等多种细胞的平衡分化及血液系统的正常循环与功能。机制上,atf7ip或setdb1缺失造成细胞周期负调节因子cdkn1a/p21与髓系转录激活因子cebpß启动子区域H3K9me3沉积减少,染色质开放程度增加,导致cdkn1a/p21和cebpß表达增加,引起造血干细胞扩增受阻,红系分化减少,最终促进髓系分化偏倚。同时,Atf7ip与Setdb1相互作用,沉默逆转录转座子(LTR/LINE)表达,抑制Mda5/Rig-I介导的天然免疫应答以及应急引起的髓系偏倚分化。该研究揭示了ATF7IP/SETDB1介导的H3K9me3沉积和染色质重塑在控制造血干细胞扩增与多种血细胞分化中的一个重要调控机制,为急性髓系白血病及其他人类疾病的干预提供了新策略 (PNAS 2022) (https://www.ecnu.edu.cn/info/1094/61875.htm)。DHX15是一种RNA解旋酶,临床发现AML患者存在DHX15 R222G突变,与AML患者不良预后相关。研究团队发现dhx15 r222g突变体呈现HSPC增殖受阻的表型,证明HSPC缺陷是通过未折叠蛋白应答(UPR)通路介导,对评估AML发生和预后具有一定临床意义(Cancer Science 2021)。
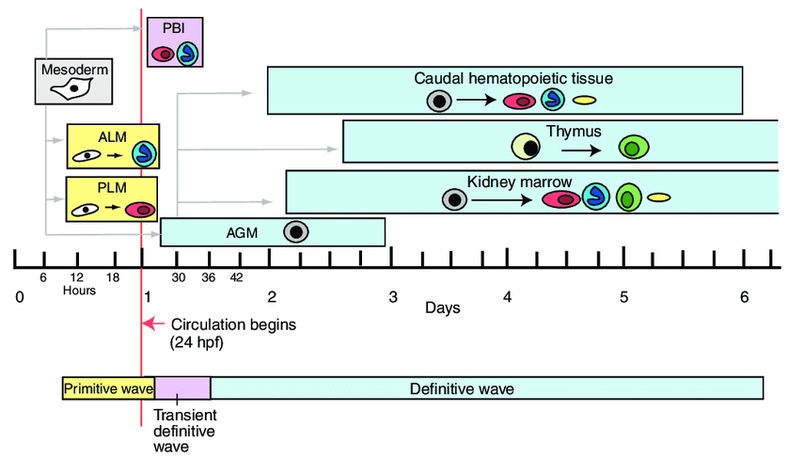
图4.斑马鱼造血过程示意图
承担科研项目情况:
主持课题有:2013年度重大科学研究计划课题;2012年国家重大科学研究计划子课题;2012年国家自然科学基金面上项目;2011年上海市浦江人才计划。在美国工作期间,钟涛教授的实验室得到美国NIH和美国心脏协会连续性的长期资助,共主持研究课题11项。
1.作为首席科学家承担2013年度重大科学研究计划发育与生殖研究领域“心肌细胞分化增殖与心脏发育的调控机制”项目。
科研成果:
钟涛教授主要以斑马鱼和小鼠为模式动物,结合人类干细胞,利用遗传学、发育生物学、化学生物学和分子生物学的方法研究心脏和血管的分化形成与再生的生物学机制。在国际科学界,第一次提出动脉血管内皮细胞在血液循环之前就已获得分子特征的概念,发现和克隆心血管发育的核心转录因子Grl/Hey2家族及其上游关键信号NOTCH通路。率先揭示了前列腺素(PGE2)信号及其转运蛋白(ABCC)调控细胞纤毛生长与心脏及多种器官形态发育的新颖生物学机制。以第一作者或通讯作者在包括Cell,Nature, Science, Nature Cell Biology等国际一流学术杂志上发表了80多篇文章。关于血管内皮细胞分化的研究成果被美国大学经典教科书《发育生物学》(第十版)采用(教科书级别重大成果)。
1.在心脏方面,发现调控心血管发育bHLH转录因子Gridlock/Hey家族,揭示Grl /Hey2与转录激活因子相互作用调节心脏生长的分子机理,为揭示房间隔缺损等相关先天性心脏病发生机制提供了分子基础。
2.在血管研究方面,揭示了动脉和静脉内皮细胞分化的分子机理,形成动静脉分化理论,被美国经典大学教科书《Developmental Biology》(Scott Gilbert编著,2010年第九版) 采用。
3.2011年回国后,发现诱导心肌细胞增殖再生的具有新型结构的小分子先导化合物(Cardinogen family)。
4.2014年,在细胞纤毛和心脏发育研究领域取得重大进展,发现前列腺素信号通路能够调控细胞纤毛生长和心脏左右不对称发育,发表于国际著名细胞生物学杂志«自然*细胞生物学»。钟涛教授在Nature、Science、Cell、PNAS等国际学术刊物发表了SCI论文逾40篇,总影响因子达390,被引用2000余次,单篇他引高达448次。
论文专著:
在Nature、Science、Cell、PNAS等国际学术刊物发表了SCI论文逾40篇,总影响因子达390,被引用2000余次,单篇他引高达448次。
代表性英文论文:
[1]Xue N, Liu X, Zhang D, Wu Y, Zhong Y, Wang J, Fan W, Jiang H, Zhu B, Ge X, Gonzalez RVL, Chen L, Zhang S, She P, Zhong Z, Sun J, Chen X, Wang L, Gu Z, Zhu P, Liu M, Li D, Zhong TP*, Zhang X*. 2023. Improving adenine and dual base editors through introduction of TadA-8e and Rad51DBD. Nature Communications. 14(1):1224. *Correspondent author
[2]Liu X, Yu T, Tan X, Jin D, Yang W, Zhang J, Dai L, He Z, Li D, Zhang Y, Liao S, Zhao J, Zhong TP*, Liu C*. 2023. Renal interstitial cells promote nephron regeneration by secreting prostaglandin E2. Elife. 12:e81438. *Correspondent author
[3]Wu J, Li J, Chen K, Liu G, Zhou Y, Chen W, Zhu X, Ni TT, Zhang B, Jin D, Li D, Kang L, Wu Y, Zhu P, Xie P, Zhong TP. 2023. Atf7ip and Setdb1 interaction orchestrates the hematopoietic stem and progenitor cell state with diverse lineage differentiation. Proc Natl Acad Sci. 120(1):e2209062120.
[4]Li D, Sun J, Zhong TP. 2022. Wnt Signaling in Heart Development and Regeneration. Curr Cardiol Rep. 24(10):1425-1438.
[5]Jin D, Zhong TP. 2022. Prostaglandin signaling in ciliogenesis and development. J Cell Physiol. 237(6):2632-2643.
[6]Liu, Xiuxiu; Pu, Wenjuan; He, Lingjuan; Li, Yan; Zhao, Huan; Li, Yi; Liu, Kuo; Huang, Xiuzhen; Weng, Wendong; Wang, Qing-Dong; Shen, Linghong; Zhong, Tao; Sun, Kun; Ardehali, Reza; He, Ben*; Zhou, Bin*.Cell proliferation fate mapping reveals regional cardiomyocyte cell-cycle activity in subendocardial muscle of left ventricle.Nature Communications, 2021, 12(1): 5784.
[7]Cai Y, Wang J, Jin D, Liu Q, Chen X, Pan L, Li Y, Wang X, Qian F, Wang J, Zhong TP*, Wang S*. 2021. Dhx15 regulates zebrafish definitive hematopoiesis through the unfolded protein response pathway. Cancer Sci. 112(9):3884-3894. *Correspondent author
[8]Wei G, Sun H, Dong K, Hu L, Wang Q, Zhuang Q, Zhu Y, Zhang X, Shao Y, Tang H, Li Z, Chen S, Lu J, Wang Y, Gan X, Zhong TP, Gui D, Hu X, Wang L, Liu J. 2021. The thermogenic activity of adjacent adipocytes fuels the progression of ccRCC and compromises anti-tumor therapeutic efficacy. Cell Metab. 33(10):2021-2039.e8.
[9]Peilu She, Huifang Zhang, Xian.gwen Peng, Jianjian Sun, Bangjun Gao, Yating Zhou, Xuejiao Zhu, Xueli Hu, Kaa Seng Lai, Jiemin Wong, Bin Zhou, Linhui Wang, Tao P. Zhong. 2020. The Gridlock/Hey2 Transcriptional Repressor Impedes Vertebrate Heart Regeneration by Restricting Expression of Lysine Methyltransferase. Development. 147(18):dev190678.
[10]Peng X, Lai KS, She P, Kang J, Wang T, Li G, Zhou Y, Sun J, Jin D, Xu X, Liao L, Liu J, Lee E, Poss KD, Zhong TP. 2021. Induction of Wnt signaling antagonists and p21-activated kinase enhances cardiomyocyte proliferation during zebrafish heart regeneration. J Mol Cell Biol. 13(1):41-58.
[11]Fang Y, Lai KS, She P, Sun J, Tao W, Zhong TP. 2020. Tbx20 Induction Promotes Zebrafish Heart Regeneration by Inducing Cardiomyocyte Dedifferentiation and Endocardial Expansion. Front Cell Dev Biol. 8:738.
[12]Sun, Yonghua; Zhang, Bo; Luo, Lingfei; Shi, De-Li; Wang, Han; Cui, Zongbin; Huang, Honghui; Cao, Ying; Shu, Xiaodong; Zhang, Wenqing; Zhou, Jianfeng; Li, Yun; Du, Jiulin; Zhao, Qingshun; Chen, Jun; Zhong, Hanbing; Zhong, Tao P.; Li, Li; Xiong, Jing-Wei; Peng, Jinrong; Xiao, Wuhan; Zhang, Jian; Yao, Jihua; Yin, Zhan; Mo, Xianming; Peng, Gang; Zhu, Jun; Chen, Yan; Zhou, Yong; Liu, Dong; Pan, Weijun; Zhang, Yiyue; Ruan, Hua; Liu, Feng; Zhu, Zuoyan; Meng, Anming; Sun, Yonghua; Pan, Luyuan. Systematic genome editing of the genes on zebrafish Chromosome 1 by CRISPR/Cas9. Genome Research, 2020, 30(1): 118-126.
[13]Zhao W, Cao L, Ying H, Zhang W, Li D, Zhu X, Xue W, Wu S, Cao M, Fu C, Qi H, Hao Y, Tang YC, Qin J, Zhong TP, Lin X, Yu L, Li X, Li L, Wu D, Pan W. 2019. Endothelial CDS2 deficiency causes VEGFA-mediated vascular regression and tumor inhibition. Cell Res. 29(11):895-910.
[14]Xie S, Fu W, Yu G, Hu X, Lai KS, Peng X, Zhou Y, Zhu X, Christov P, Sawyer L, Ni TT, Sulikowski GA, Yang Z, Lee E, Zeng C, Wang WE, Zhong TP*. Discovering small molecules as Wnt inhibitors that promote heart regeneration and injury repair. Journal of Molecular Cell Biology, 2020, 12(1): 42-54.
[15]Li G, Jin D, Zhong TP. 2019. Tubgcp3 Is Required for Retinal Progenitor Cell Proliferation During Development. Frontier in Mol Neurosci. 12:126
[16]Li, Wenyan; Jin, Daqing*; Zhong, Tao P*.Photoreceptor cell development requires prostaglandin signaling in the zebrafish retina. Biochemical and Biophysical Research Communications, 2019, 510(2): 230-235.
[17]Zhang Ruilin; He Jie; Wang Xu; Pan Weijun; Cao Ying; Zu Yao; Jiang Qiu; Du Jiulin; Zhong Tao P.Report of the Fifth Zebrafish Research Conference of China.Zebrafish, 2019, 16(1): 128-134.
[18]Yang, Xinyu; Li, Jiani; Fang, Yabo; Zhang, Zhen; Jin, Daqing; Chen, Xingdong; Zhao, Yan; Li, Mengqi; Huan, Linchun; Kent, Thomas A.; Dong, Jing-Fei; Jiang, Rongcai; Yang, Shuyuan; Jin, Li; Zhang, Jianning*; Zhong, Tao P.*; Yu, Fuli*. Rho Guanine Nucleotide Exchange Factor ARHGEF17 is a risk gene for Intracranial Aneurysms. Circulation-Genomic and Precision Medicine, 2018, 11(7): e002099. *Correspondent author
[19]Daqing Jin, Diqi Zhu, Yabo Fang, Yiwei Chen, Gaihong Yu, Weijun Pan, Dong Liu, Fen Li, Zhong TP. 2017. Vegfa signaling regulates diverse artery/vein formation in vertebrate vasculatures. J Genet Genomics. 44(10):483-492
[20]Xueying Tian, Yan Li, Lingjuan He, Hui Zhang, Xiuzhen Huang, Qiaozhen Liu, WenjuanPu, Libo Zhang, Yi Li, Huan Zhao, Zhifu Wang, Jianhong Zhu, Yu Nie, Shengshou Hu, David Sedmera, Zhong TP, Sean Wu, William Pu, Robert Anderson, Bin Zhou, Ying Yu, Li Zhang, Yan Yan, Zengyong Qiao, and Qing-Dong Wang. 2017. Identification of a hybrid myocardial zone in the mammalian heart after birth. Nature Communications. 8(1):87.
[21]Zeng S., Zhong TP. 2017. Cardioascular Research in Zebrafish. Encyclopedia of Cardiovascular Research and Medicine. vol 4. p759-770. Vasan R, Sawyer D ed. Oxford: Elsevier,inc.
[22]Peiyun Liu, Zhong TP*. 2017. MAPK/ERK signalling is required for zebrafish cardiac regeneration. Biotechnology Letters, 2017, 39(7): 1069-1077.
[23]Diqi Zhu, Yabo Fang, Kun Gao, Jie Shen, Zhong TP+ and Fen Li+. 2017. Vegfa Impacts Early Myocardium Development. Int J Mol Sci. 18(2). +Correspondent author
[24]Da Wo, Jinhui Peng, Dan-ni Ren, Liman Qiu, Jinxiao Chen, Ye Zhu, Yingjing Yan,Hongwei Yan, Jian Wu, En Ma, Zhong TP, Yi-Han Chen, Zhong-Min Liu, Shangfeng Liu, Luoquan Ao, Zhenping Liu, Cizhong Jiang, Jun Peng, Yunzeng Zou, Qirong Qian, Weidong Zhu. 2016. Opposing Roles of Wnt Inhibitors IGFBP-4 and Dkk1 in Cardiac Ischemia by Differential Targeting of LRP5/6 and β–catenin. Circulation. 134(24):1991-2007.
[25]Sun Jianjian, Zhihan Wu and Zhong TP. 2016. Cila Function in Cell Signaling and Organ Development. Scientia Sinica Vitae. 46,4:354-62
[26]Peng Xiangwen; He Quanze; Li Guobao; Ma Jinmin; Zhong Tao P*. Rac1-PAK2 pathway is essential for heart regeneration. Biochemical and Biophysical Research Communications, 2016, 472(4): 637-642.
[27]Li, Qiao; Yang, Hao; Zhong, Tao P*. Regeneration across Metazoan Phylogeny: Lessons from Model Organisms. J Genet Genomics. 42:57-70.
[28]Nan Wu, Xuan Ming, Jianqiu Xiao, Zhihong Wu, Xiaoli Chen, Marwan Shinawi, Yiping Shen, Guangju Yu, Jiaqi Liu, Hua Xie, Zoran S. Gucev, Sen Liu, Nan Yang, Hussam Al-Kateb, Jun Chen, Jian Zhang, Natalie Hauser, Ting Zhang, Velibor Tasic, Pengfei Liu, Xinlin Su, Xuedong Pan, Chunyu Liu, Liwen Wang, Joseph Shen, Jianxiong Shen, Yulin Chen, Ting Zhang, Jianguo Zhang, Kwong Wai Choy, Jun Wang, Qiqi Wang, Shugang Li, Weichen Zhou, Jin Guo, Yipeng Wang, Cheng Zhang, Hong Zhao, Yu An, Yu Zhao, Jiucun Wang, Zhenlei Liu, Yuzhi Zuo, V. Reid Sutton, Hongyan Wang, Yue Ming, Shashikant Kulkarni, Zhong TP, Sau Wai Cheung,Xue Zhang, Li Jin, James R. Lupski, Guixing Qiu, and Feng Zhang. 2015. Compound Inheritance of TBX6 Rare Null Variants and a Common Hypomorphic Allele in Congenital Scoliosis. New England Journal of Medicine. 372(4):341-50.
[29]Jin D, Liu PY, Zhong TP. 2015. Prostaglandin Signaling in Ciliogenesis during Development. Cell Cycle. 14 (1):1-2.
[30]Tian, Xueying; Hu, Tianyuan; Zhang, Hui; He, Lingjuan; Huang, Xiuzhen; Liu, Qiaozhen; Yu, Wei; He, Liang; Yang, Zhen; Yan, Yan; Yang, Xiao; Zhong, Tao P; Pu, William T; Zhou, Bin. De Novo formation of a distinct coronary vascular population in neonatal heart. Science, 2014, 345(6192): 90-94..
[31]Du, Xingrong; Shi, Hao; Li, Jiang; Dong, Yongli; Liang, JieLiang; Ye, Jian; Kong, Shanshan; Zhang, Shujing; Zhong, Tao; Yuan, Zengqiang; Xu, Tian; Zhuang, Yuan; Zheng, Biao; Geng, Jian-Guo; Tao, Wufan. Mst1/Mst2 regulate development and function of regulatory T cells through modulation of Foxo1/Foxo3 stability in autoimmune disease. The Journal of Immunology, 2014, 192(4): 1525-1535.
[32]Jin D, Ni TT, Sun J, Wan H, Amack JD, Yu G, Fleming J, Chiang C, Li W, Papierniak A, Cheepala S, Conseil G, Cole SP, Zhou B, Drummond IA, Schuetz JD, Malicki J, Zhong TP. 2014. Prostaglandin signaling regulates ciliogenesis and heart development by modulating intraflagellar transport. Nature Cell Biology.16 (9):841-51. (Article & Cover story; Previews by Barbry P & Zaragosi L E : An ABC of ciliogenesis. 2014. Nature Cell Biololgy. 16(9):826-7).
[33]Dai X, She P, Chi F, Feng Y, Liu H, Jin D, Zhao Y, Guo X, Jiang D, Guan KL, Zhong TP, Zhao B. 2013. Phosphorylation of angiomotin by Lats1/2 kinases inhibits F-actin binding, cell migration and angiogenesis. J Biol Chem. 288 (47):34041-51.
[34]Sun YP, Dong ZQ, Jin TH, Ang KK, Huang M, Haston KM, Peng J, Zhong TP, Finkbeiner, S, Weiss WA, Jan LY, Guo S. 2013. Imaging-based chemical screening reveals activity-dependent neural differentiation of pluripotent stem cells. Elife. e00508 (HHMI Press)
[35]Cheepala SB, Bao J, Nachagari D, Sun D, Wang Y, Zhong TP, Naren AP, Zheng J, Schuetz JD. 2013. Crucial role for phylogenetically conserved cytoplasmic loop3 inABCC4 expression. J Biol Chem. 288(31):22207-18.
[36]Tian X, Hu T, Zhang H, He L, Huang X, Liu Q, Yu W, He L, Yang Z, Zhang Z, Zhong TP, Yang X, Yang Z, Yan Y, Baldini A, Sun Y, Lu J, Schwartz RJ, Evans SM, Gittenberger-de Groot AC, Red-Horse K, Zhou B. 2013. Subepicardial endothelial cells invade the embryonic ventricle wall to form coronary arteries. Cell Research. 14 (5):371-45 (NaturePress)
[37]Xiang Y, Cho PH, Zeng X, Zheng XJ, Jessen JR, Zhong TP, Xu XL. 2013. Trapping Cardiac Recessive Mutants via Expression-based Insertional Mutagenesis Screening. Circulation Research. 112 (4):606-17
[38]Jin DQ, Li Q and Zhong TP. 2013. Chemical Genetics in Cardiomyocyte Generation. Chapter III in “Chemical Biology in Regenerative Medicine: Bridging Stem Cells and Future Therapies”. Wiley Publication, inc. USA
[39]Ni TT, Lu J, Zhu M, Maddison LA, Boyd KL, Huskey L, Ju B, Hesselson D, Zhong TP, Page- McCaw PS, Stainier DY, Chen W. 2012. Conditional control of gene function by an invertible gene trap in zebrafish. Proc Natl Acad Sci. 109:15389-94.
[40]Ni, Terri T; Rellinger, Eric J; Mukherjee, Amrita; Xie, Shuying; Stephens, Lauren; Thorne, Curtis A; Kim, Kwangho; Hu, Jiangyong; Lee, Ethan; Marnett, Larry; Hatzopoulos, Antonis K; Zhong, Tao P*. Discovering small molecules that promote cardiomyocyte generation via modulating Wnt signaling. Chemistry & Biology. 8:1658-1668 (CellPress). (Previews by Ruey J. Yeh: A Wnt Inhibitors with a Twist. Chemistry & Biology. 18:1518-1520, 2011; Lab Reports, JAMA 307:5, 446, 2012)
[41]Chopra SS, Watanabe V, Yang T, Stroud DM, Burns CG, Wells S, Zhong TP+, Roden DM. 2010. A non-electrogenic requirement for voltage-gated sodium channels in zebrafish heart development. Circulation Research. 106:1342-50. +Correspondent author
[42]Williams, Charles; Kim, Seok-Hyung; Ni, Terri T; Mitchell, Lauren; Ro, Hyunju; Penn, John S; Baldwin, Scott H; Solnica-Krezel, Lila; Zhong, Tao P*. Hedgehog signaling induces arterial endothelial cell formation by repressing venous cell fate. Developmental Biology, 2010, 341(1): 196-204.
[43]Jin D, Ni TT, Hou J, Rellinger E, Zhong TP. 2009. Promoter analysis of ventricular myosin heavy chain (vmhc) in zebrafish embryos. Developmental Dynamics. 238,1760-1767
[44]Zeng X, Zheng XJ, Xiang Y, Cho PH, Jessen JR, Zhong TP, Solnica-Krezel L and Brown AL. 2009. Phospholipase D1 is required for angiogenesis of intersegmental blood vessels in zebrafish. Developmental Biology. 328,363-76
[45]Ni TT, William L, Shyr Y, Zhong TP. 2008. Use of normalization methods for analysis of microarrays containing ahigh degree of gene effects. BMC Bioinformatics. 9, 505.
[46]Qu XH, Jia HB, Garrity DM, Tompkins K, Batts L, Appel B, Zhong TP+, Baldwin S. 2008. Ndrg4is required for normal myocyte proliferation during early cardiac development in zebrafish. Developmental Biology. 317, 486-96. +Correspondent author
[47]Wang YX, Qian LX, Liu D, Yao LL, Gui YH, Zhong TP. Song HY. 2007. Bone morphogenetic protein-2 acts upstream of myocyte-specific enhancer factor 2a to control embryonic cardiac contractility. Cardiovascular Research. 74 (2):290-303.
[48]Chopra S, Hiroshi Watanable, Zhong TP+, Roden D. 2007. Molecular cloning and analysis of zebrafish voltage-gated sodium channel b-subunits: Implication for the evolution of electrical signaling in vertebrates. BMC Evolution Biology. 7, 113-7. +Correspondent author.
[49]Chopra S and Zhong TP. 2007. Vascular Development in Zebrafish. Endothelial Biomedicine. 1107-1127. Cambridge: Cambridge University Press, UK.
[50]Jia H, King I, Chopra S, Wan H, Ni T, Jiang C, Guan X, Well S, Srivastava D and Zhong TP. 2007. Vertebrate heart growth is regulated by functional antagonism between Gridlock and Gata5. Proc Natl Acad Sci. 104,14008-14013.
[51]Campbell WA, Yang H, Zetterberg H, Baulac S, Sears JA, Liu T, Wong STC, Zhong TP, XiaW. 2006. Zebrafish lacking Alzheimer presenilin enhancer 2 (Pen-2) demonstrate excessive p53 dependent apoptosis and neuronal loss. J Neurochemistry. 96,1423-40.
[52]Rutenberg JB, Fischer A., Jia HB, Gessler M., Zhong TP and Mercola M. 2006. Developmental patterning of the cardiac atrioventricular canal by Notch and Hairy-related transcription factors. Development. 133,4381-90.
[53]Wang Y, Zhong TP, Qian L, Dong Y, Jiang Q, Tan L, Song H. 2005. Wortmannin induces zebrafish cardia bifida through a mechanism independent of phosphoinositide 3-kinase and myocisn light chain kinase. Biochem Biophys Res Commun. 331 (1):303-8
[54]Zhang L, Zhong TP, Wang Y, Jiang Q, Song H, Gui Y. 2005. TBX1, a DiGeorge syndrome candidate gene, is inhibited by retinoic acid. Int. J. Developmental Biology. 50:55-61
[55]Wang Y, Qian L, Zhang Y, Jiang Q, Dong Y, Liu X, Yang X, Zhong TP+, Song H. 2005. Requirements of myocyte-specific enhancer factor 2A in zebrafish cardiac contractility. FEBS. 579, 4843-50. +Correspondent author
[56]Zhong TP. 2005. Zebrafish Genetics and Formation of Embryonic Vasculature. Current Topics in Development Biology. 71,53-81.
[57]Peterson R, Shaw SY, Peterson TA, Milan DJ, Zhong Tao P, Schreiber S, Mac Rae C and Fishman, MC. 2004. Chemical suppression of a genetic mutation in a zebrafish model of aortic coarctation. Nature Biotechnology. 22, 593-599.
[58]Xu X, Miller S, Zhong TP, Mohideen M, Crossley DA, Burggren WW and Fishman MC. 2002. Cardiomyopathy in zebrafish due to mutation in an alternatively spliced exon of Titin. Nature Genetics. 30, 205-209.
[59]Zhong TP, Childes S, Leu J, Fishman MC. 2001. The Gridlock signaling pathway fashions the first embryonic artery. Nature. 414, 216-220. (Comment by George D. Yancopoulos: Gridlock in the blood. Nature. 404, 163-164)
[60]Zhong TP, Rosenberg M, Mohideen M, Weinstein B, Fishman MC. 2000. Gridlock, an HLH gene required for assembly of the aorta in zebrafish. Science. 287, 1820-1824.
[61]Amemiya C, Zhong TP, Silverman G, Fishman MC, Zon L. 1999. In the zebrafish: Genetics and Genomics. Methods in Cell Biol. H.W. Detrich, III, M. Westerfield, L.I. Zon, Eds. (Academic Press, San Diego) pp.236.
[62]Zhong TP, Kaphingst K, Akella U, Haldi M, Lander E and Fishman MC. 1998. Zebrafish genomic library in yeast artificial chromosome. Genomics. 48, 136-138.
[63]Zhong TP, Luke M and Arndt K. 1996. Transcriptional regulation of the yeast DnaJ molecule SIS1 gene. J. Biological Chemistry. 271, 1349-1356.
[64]Zhong TP and Arndt K. 1993. Yeast SIS1 protein, a DnaJ homologue, is required for the Initiation of translation. Cell. 73, 1175-1186.
[65]Sarabia M, Sutton A, Zhong TP and Arndt K. 1992. SIT4 protein phosphatase is required for the normal accumulation of SWI4, CLN1, CLN2, and HCS26 RNAs during Late G1. Genes & Development. 6, 2417-2428.
代表性中文论文:
[1]孙建建; 钟涛; 朱平*.Cardiac fibrosis: Histological features, molecular pathways and therapeutic targets.South China Journal of Cardiology, 2022, 23(02): 115-128.
[2]张琳; 靳大庆*; 钟涛*.斑马鱼皮肤黑色素小体聚集和分散的机制研究.生物学教学, 2022, 47(10): 2-5.
[3]刘旭; 仲祉霖; 钟涛*.碱基编辑器的研发及其应用.中国细胞生物学学报, 2022, 44(12): 2294-2304.
[4]孙建建, 武子涵, 钟涛. 细胞纤毛在信号转导与器官发育中的作用与机制[J]. 中国科学:生命科学, 2016, 46 (04): 354-362.
[5]孙淑娜, 桂永浩, 蒋璆, 宋后燕, 钟涛. 叶酸缺乏对斑马鱼胚胎造血系统影响的初步研究[J]. 营养学报, 2010, 32 (01): 21-25.
[6]孙淑娜, 桂永浩, 宋后燕, 钟涛, 王跃祥, 蒋璆. 叶酸拮抗剂甲氨喋呤导致斑马鱼心脏发育异常及BMP2b HAS2表达下调[J]. 中国当代儿科杂志, 2007, (02): 159-163.
[7]张立凤, 桂永浩, 钟涛, 王跃祥, 钱林溪, 董永新, 蒋璆, 孙淑娜, 宋后燕. 外源性视黄酸对斑马鱼Tbx1基因的影响[J]. 中华儿科杂志, 2007, 45 (04): 267-271.
[8]张立凤, 桂永浩, 钟涛, 王跃祥, 蒋球, 崇梅, 孙淑娜, 宋后燕. 视黄酸影响斑马鱼胚胎心脏房室分化[J]. 复旦学报(医学版), 2007, (01): 88-91.
[9]张立凤, 钟涛, 桂永浩. 外源性视黄酸对斑马鱼心血管系统发育的影响[J]. 中国实验动物学报, 2006, (02): 84-88+73-74.
[10]刘学飞, 王跃祥, 蒋璆, 钱林溪, 高广文, 董永新, 钟涛, 宋后燕. 斑马鱼胚胎发育过程中Mef2c的表达[J]. 复旦学报(医学版), 2006, (01): 89-91+143.
[11]钱林溪,王跃祥,蒋璆,钟涛,宋后燕. 乙醇干扰斑马鱼胚胎发育中底索和背主动脉的形成[J]. 中国科学(C辑:生命科学), 2005, (04): 326-332.
[12]钱林溪,钟涛,宋后燕. 斑马鱼早期内胚层发育及其分子调控机制[J]. 生命的化学, 2005, (04): 297-299.
[13]王跃祥,钟涛,宋后燕. 斑马鱼发育遗传学研究进展[J]. 国外医学.遗传学分册, 2004, (04): 220-223.
[14]高广文,钟涛,宋后燕. 斑马鱼外胚层早期发育及其某些调控机制[J]. 生命的化学, 2004, (03): 227-229.
[15]陈新明,钟涛,万钧,吴杰,张世永. WWW搜索引擎的数据采集技术[J]. 计算机工程与应用, 2002, (07): 145-147+161.
[16]钟涛,李微刚,张世永. 基于高速IP网的远程教育系统[J]. 计算机工程与应用, 2001, (20): 126-128.
[17]钟涛,陈新明,万钧,张世永. 中文文本WEB搜索引擎的设计与实现[J]. 计算机工程与应用, 2001, (17): 149-151+169.
会议论文:
[1]钟涛. (2014). Regulation of vertebrate ciliogenesis and heart development. (eds.) 第三届“模式生物与人类健康”发育遗传学全国学术研讨会论文集 (pp.78).
[2]侯佳, 桂永浩, 张立凤, 王跃祥, 宋后燕 & 钟涛. (2008). 视黄酸缺乏对斑马鱼胚胎心脏发育的影响. (eds.) 中华医学会第五次全国儿科中青年学术交流大会论文汇编(上册) (pp.440-448).
[3]孙淑娜, 桂永浩, 蒋璎, 宋后燕 & 钟涛. (2008). 叶酸对斑马鱼胚胎心脏发育影响的实验研究. (eds.) 中华医学会第五次全国儿科中青年学术交流大会论文汇编(上册) (pp.470-477).
[4]孙淑娜, 宋后燕, 钟涛, 王跃祥 & 桂永浩. (2006). 叶酸缺乏导致先天性心血管疾病的实验动物研究. (eds.) 2006(第三届)江浙沪儿科学术会议暨浙江省儿科学术年会论文汇编 (pp.197).
[5]张立凤,桂永浩,钟涛,王跃祥,蒋球,崇梅... & 宋后燕. (2006). 视黄酸影响胚胎心脏房室分化的实验研究. (eds.) 2006(第三届)江浙沪儿科学术会议暨浙江省儿科学术年会论文汇编 (pp.211).
[6]张立凤,桂永浩,王跃祥,钱林溪,董永新,蒋璆... & 宋后燕. (2006). Tbx1基因影响胚胎咽弓和心脏发育的实验研究. (eds.) 2006(第三届)江浙沪儿科学术会议暨浙江省儿科学术年会论文汇编 (pp.211-212).
[7]孙淑娜, 桂永浩, 宋后燕, 王跃祥 & 钟涛. (2006). 叶酸缺乏导致先天性心血管疾病的实验动物研究. (eds.) 中华医学会第十四次全国儿科学术会议论文汇编 (pp.456-457).
团队成员:
教授:钟涛
副教授:靳大庆、李东亮
博士后:佘培露、孙建建、胡雪丽
博士研究生:高邦君、朱雪娇、周亚婷、吴佳欣、李娟、刘旭、陈业伟
硕士研究生:贺渊、张琳、苗婷婷、强梦轲、仲祉霖、陈雯琪、万萌、史西亚、漆瑶、莫菲、张人杰
团队活动



学生荣誉:



荣誉奖励:
1. 上海“**计划”专家。
2. 国家杰出青年科学基金奖(B类)。
3. 科学中国人(2014)年度人物。
4. 施李月卿杰出毕业生(原上海医科大学)。
5. American Heart Association Research Awards.
6. March of Dimes Research Award (USA).
7. NIH Grant Awards (USA).
8. NIH Postdoctoral Fellowship (USA).
第三场博思青年学者讲坛成功举行
2013年9月15日,博思讲坛第三场青年学者讲坛在立人生物楼107室举行,拉开了新学期博思讲坛系列活动的帷幕。此次青年学者讲坛邀请到了来自中科院上海生化与细胞所的顾天鹏、施小山;来自中科院上海生命科学院健康所的宋昕阳和来自第二军医大学的冯家烜与复旦大学生命科学学院的同学们分享科研成果与经验。这四位同学均是被誉为华人生物学在读博士最高奖项的吴瑞奖学金得主。

首先,生命科学学院的钟涛教授致辞,勉励同学做科研要有全心全意的投入精神、大胆的创新精神和积极主动的交流合作能力,并努力向兄弟院校的优秀博士生学习。
接下来,宋昕阳博士以“肠道抗感染免疫中的新白介素及其受体”为题,介绍了新型白介素17受体E的发现过程和它在肠道抗感染免疫中的功能,并介绍失调的肠道菌群通过白介素17C的表达促进肠道肿瘤的发生作用机制。施小山做了“钙离子调控T细胞抗原受体活化的机制”的报告,他向大家展示了钙离子可以在T细胞初始刺激后调控细胞质膜的带电性,最终促进适应性免疫功能开启的证据。顾天鹏则介绍了早期胚胎发育过程中受精卵内雄核源DNA主动去甲基化发生机制及其生物学意义。冯家烜展示了他关于主动脉夹层腔内支架改进和动脉内膜生物力学研究的创新成果。
在最后的互动提问环节,大家探讨了如何应对科研过程中遇到的困难、如何建立自信心、研究生新生如何做好研究和学习的规划等问题。四位演讲者以亲身经历告诉大家,研究生学习的早期重心应放在知识的储备和能力的提升上;先动脑再动手,效率高;遇到困难不要轻易放弃,学会创造条件,让自己的结果得到认可;要乐于同他人交流分享,积极合作。同学们表示听了他们的报告,很受鼓舞,更加坚定了努力科研的决心。

博思讲坛成立于2012年11月,是由复旦大学生命科学学院研究生发起,遗传工程国家重点实验室经费支持,学生自主推选和邀请生命科学领域杰出科学家(大师讲坛)和优秀学生代表(青年学者讲坛)与学生交流的论坛。从成立至今已经举办十几场活动,为生命科学领域的研究生搭建了一个良好的学术交流平台。
来源:复旦大学生命科学学院 2013-09-18
中国科技创新人物云平台暨“互联网+”科技创新人物开放共享平台(简称:中国科技创新人物云平台)免责声明:
1、中国科技创新人物云平台是:“互联网+科技创新人物”的大型云平台,平台主要发挥互联网在生产要素配置中的优化和集成作用,将互联网与科技创新人物的创新成果深度融合于经济社会各领域之中,提升实体经济的创新力和生产力,形成更广泛的以互联网为基础设施和实现工具的经济发展新形态,实现融合创新,为大众创业,万众创新提供智力支持,为产业智能化提供支撑,加快形成经济发展新动能,促进国民经济提质增效升级。
2、中国科技创新人物云平台暨“互联网+”科技创新人物开放共享平台内容来源于互联网,信息都是采用计算机手段与相关数据库信息自动匹配提取数据生成,并不意味着赞同其观点或证实其内容的真实性,如果发现信息存在错误或者偏差,欢迎随时与我们联系,以便进行更新完善。
3、如果您认为本词条还有待完善,请编辑词条。
4、如果发现中国科技创新人物云平台提供的内容有误或转载稿涉及版权等问题,请及时向本站反馈,网站编辑部邮箱:kjcxac@126.com。
5、中国科技创新人物云平台建设中尽最大努力保证数据的真实可靠,但由于一些信息难于确认不可避免产生错误。因此,平台信息仅供参考,对于使用平台信息而引起的任何争议,平台概不承担任何责任。

















