光寿红,中国科学技术大学生命科学院教授、博士生导师,中组部"青年**计划"首批入选者,中国科学院"**计划"入选者。长期从事遗传学和分子生物学相关研究,于2011年建立中国科学技术大学分子遗传学实验室。
教育及工作经历:
1996年,在中国科学技术大学生物系获得学士学位。
1996-1999年,师从中国科大施蕴渝院士进行多肽的溶液构象研究,并获得硕士学位。
1999-2004年,在美国威斯康星大学癌症研究所师从Janet Mertz教授,研究真核生物中病毒起源的无内含子RNA的表达和调控机制,并获得博士学位。
2005-2010年,作为博士后在威斯康星大学遗传系Scott Kennedy助理教授实验室,从事模式生物中小干扰RNA的功能和调控机理的研究。进一步研究小干扰RNA的功能和调控机制。
主讲课程:
资料更新中……
培养研究生情况:
资料更新中……
招聘情况:
一、博士后,助理研究员
1.近年获博士学位(助理研究员可为硕士学位),有志从事科学研究;
2.拥有良好的分子生物学、细胞生物学、发育生物学或医学等相关专业背景;
3.在SCI刊物上至少发表过一篇第一作者论文;
4.富有独立工作能力、责任心和协作精神;
5.思想开放, 乐于学习和接受新事物,懂得为前途而打拼。
二、特任副教授,特任副研究员
1.博士学位并有不少于两年的相关生物博士后研究经验;
2.拥有以下1-2项深入的研究经验并有一定建树:分子生物学、细胞生物学、遗传学。
3.在SCI刊物上发表过多篇篇较高水平第一作者论文、有独立撰写学术论文和申请经费能力;
4.具有独立领导研究生开展子课题研究的能力。
5.提供2位或以上同行专家详细联系方式。
受聘者将获得与课题相关的基础和研究训练,相对独立地承担相关的科研工作,协助指导研究生,申请科研经费。应聘者的申请材料严格保密。初审通过者将安排面试,面试时间另行通知。应聘者被正式录用后,其工资等有关待遇按照学校相关政策制度执行。优秀者有额外补贴。本实验室鼓励并支持年轻人在科学上发展并逐渐独立。
此招聘长期有效。请应聘者将个人简历和个人计划通过电子邮件发送至:sguang@@@ustc.edu.cn
研究方向:
长期从事遗传学和分子生物学相关研究。
(1)真核细胞中RNA的表达与加工的调节;
(2)真核生物中转录调节机制;
(3)非编码RNA的表达与调节机制;
(4)模式生物的遗传与发育;
(5) 基因编辑和染色体操纵的新技术和新方法。
承担科研项目情况:
承担973和基金委课题,同时获中组部青年**计划和中科院**计划资助。
申请过两个国家自然科学基金的面上项目:一个是研究非编码核糖核酸在生物体中的作用机制,另一个是非编码核糖核酸造成错靶效应的机制。
本实验室是在模式生物秀丽线虫里进一步研究小RNA 和RNA干扰对干细胞发育和分化的功能及调节机制。具体而言,包括干细胞发育和分化过程中核RNA干扰途径的内在功能,内源性小RNA的产生,以及RNA干扰的错靶现象的机理。这项研究不仅对理解小RNA和干细胞的基础生物学关系有重要意义,而且有助于更好地将小RNA和干细胞应用于研究和临床治疗的原因和机理。
1. 核RNA干扰通路的内在功能。在干细胞的发育和分化过程中,小RNA介导的基因表达调控是非常重要的,然而,其具体作用机制还不清楚。我们的初步研究表明,NRDE介导的小RNA核干扰途径对秀丽线虫干细胞的发育和分化是非常必要的。因此,要进一步了解核RNA干扰途径在此过程中的生理功能,我们必须首先寻找核RNA干扰的内在靶位,以及整个核RNA干扰途径的体系构造。
我们计划使用基因组测序的方法来: (A) 确认nrde通路调控的基因序列;(B)确认NRDE-2和NRDE-3直接结合的前RNA的序列;(C) 确认NRDE-3结合的小RNA的序列。那些同时被这三种方法检测到的基因才可能是核RNA干扰途径的真正调控靶位。接下来我们计划使用已经建立的遗传和生化方法来进一步证实它们的表达受nrde通路的调控,以及研究这个调控是如何进行的。寻找和阐明这些核RNA的调控靶位可以让我们更深入地研究nrde突变体里干细胞发育和分化缺陷。
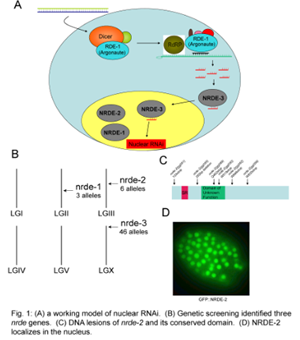
2. 内源性小RNA的产生机理。动物体内小RNA的产生是一个精密调节的过程。异常的小RNA的表达往往会造成很多发育缺陷,例如癌症和生殖不育以及干细胞定向分化和发育的缺陷。然而,迄今为止小RNA的产生机制并不清楚。我们已经建立了一个高效的遗传筛选方法来研究在线虫里的小RNA的产生机理:NRDE-3在细胞内的定位取决于它是否结合小RNA。当结合小RNA的时候,NRDE-3定位于细胞核,如果不结合小RNA的时候,NRDE-3定位于细胞质。通过对NRDE-3的定位研究,我们发现在一些突变体内,NRDE-3可以结合异常的小RNA,这些小RNA在野生型动物中往往很难被检测到。我们推测这些突变体基因应该是小RNA表达的负调控基因。 我们计划进一步克隆这些突变体基因以及它们调控的小RNA,从而了解其作用机制。这项研究必将有助于我们更好地了解小RNA的产生和调节机制,从而帮助我们更好地了解人类疾病的产生原因,特别是在干细胞的发育和分化过程中小RNA的内在功能。
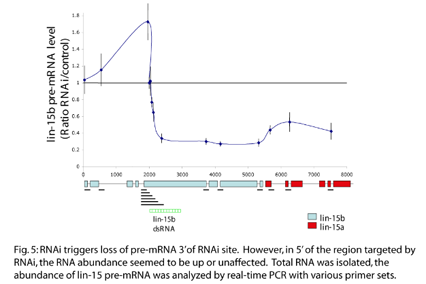
3. RNA干扰的错靶现象的机理。在将小RNA干扰技术运用于科学研究和疾病治疗的过程中,RNA干扰的错靶现象是研究人员都担心和正在研究的关键问题。通常的观念认为碱基的错配是不可避免的,从而造成错靶现象。然而,我们在研究中发现,一些RNA干扰的错靶现象是主动地遗传调控过程,而且这种错靶现象与核RNA干扰途径紧密相关。例如,错靶的小RNA会优先结合NRDE-3,运输到核里,诱导组蛋白3的9位赖氨酸(H3K9)的甲基化。
我们计划进一步通过一系列的遗传和生化的方法来研究RNA干扰的错靶现象的机理。例如,(1)通过RNA免疫沉淀(RIP)的方法,辨别错靶是起源于细胞质还是细胞核;(2)通过深度测序,阐明造成错靶现象的小RNA是否在序列和结构上有特异性;(3)为了进一步研究错靶现象的机理,我们已通过遗传筛选的方法发现了多个抑制错靶现象的突变体。通过克隆这些突变体基因,我们希望可以揭示错靶现象的产生和作用机理,从而帮助我们更好地设计和运用基于小RNA干扰的药物。
科研成果:
1.在包括Nature和Science在内的国际著名期刊上发表论文12篇(其中第一作者6篇),2篇论文被Faculty of 1000 Biology收录并给予高度评价,曾获得中国科学院院长奖及美国心脏协会博士后奖。
2.发现真核生物中无内含子的基因含有一些顺式作用的RNA序列元素,它们可以和细胞内的特定蛋白相互结合,来提高该无内含子基因的前mRNA的稳定性,poly(A)聚腺苷酸化,以及从细胞核到细胞质的运输;发现这些结合蛋白在正常情况下应用于含内含子的内源性基因的表达和加工。这项研究指出无内含子基因可以把细胞内正常基因表达和加工的所需因子转为己用。此研究为治疗病毒感染和癌症提供了新的思路(NAR 2005; MCB 2005)。
3.确认了高等动物中存在着细胞核里的基因干扰现象;发现了非编码RNA从细胞质转运到细胞核的新途径;发现了三个nrde基因;证明了非编码的小RNA可以结合到正在被转录的转录子上;发现细胞核RNA干扰的机理可能是通过抑制RNA聚合酶II,抑制转录的延伸,从而造成转录的提前终止;发现高等动物中非编码的小干扰RNA可以造成组蛋白的甲基化,而且这部分甲基化完全依赖于nrde基因;发展了模式生物整体上RNA-蛋白的免疫沉淀方法;发展了模式生物整体水平上转录活性的测量方法(Science, 2008;Nature, 2010)。
在包括Nature和Science在内的国际著名期刊上发表论文12篇(其中第一作者6篇),2篇论文被Faculty of 1000 Biology收录并给予高度评价。
代表性英文论文:
[1] Minjie Hong(#), Xiaotian Zhou(#), Chenming Zeng, Demin Xu, Ting Xu, Shimiao Liao, Ke Wang, Chengming Zhu, Ge Shan, Xinya Huang(*), Xiangyang Chen(*), Xuezhu Feng(*) & Shouhong Guang(*) (2024b) Nucleolar stress induces nucleolar stress body formation via the NOSR-1/NUMR-1 axis in Caenorhabditis elegans. Nature Communications, 2024 volume 15, Aug 23 https://doi.org/10.1038/s41467-024-51693-z
[2] Xiangyang Chen(#), Ke Wang(#), Farees Ud Din Mufti(#), Demin Xu, Chengming Zhu, Xinya Huang, Chenming Zeng, Qile Jin, Xiaona Huang, Yong-hong Yan, Meng-qiu Dong, Xuezhu Feng(*), Yunyu Shi(*), Scott Kennedy(*) & Shouhong Guang(*) (2024a) Germ granule compartments coordinate specialized small RNA production. Nature Communications, 15, 5799 (2024). https://doi.org/10.1038/s41467-024-50027-3
[3] Ling Liu, Yifan Wu, Ke Liu, Mengdan Zhu, Shouhong Guang, Fengsong Wang, Xing Liu, Xuebiao Yao, Jiajia He(*), Chuanhai Fu(*) (2024) The absence of the ribosomal protein Rpl2702 elicits the MAPK-mTOR signaling to modulate mitochondrial morphology and functions. Redox Biol. 2024 Apr 29:73:103174. doi: 10.1016/j.redox.2024.103174.
[4]Wei I Jiang, Henry De Belly, Bingying Wang, Andrew Wong, Minseo Kim, Fiona Oh, Jason DeGeorge, Xinya Huang, Shouhong Guang, Orion D Weiner, Dengke K Ma (2024) Early-life stress triggers long-lasting organismal resilience and longevity via tetraspanin Science Advance 2024 Jan 26;10(4):eadj3880. doi: 10.1126/sciadv.adj3880. Epub 2024 Jan 24.
[5]Ruofan Ding, Xudong Zou, Yangmei Qin, Lihai Gong, Hui Chen, Xuelian Ma, Shouhong Guang, Chen Yu, Gao Wang, Lei Li (2023) xQTLbiolinks: a comprehensive and scalable tool for integrative analysis of molecular QTLs. Brief Bioinform. 2023 Nov 22;25(1):bbad440. doi: 10.1093/bib/bbad440.
[6]Pandey T, Kalluraya CA, Wang B, Xu T, Huang X, Shouhong Guang, Daugherty MD, Ma DK (*) (2023) Acquired stress resilience through bacteria-to-nematode interdomain horizontal gene transfer. EMBO J. (2023b) Nov 13:e114835. doi: 10.15252/embj.2023114835.
[7]Zhiwen Zhu(#), Dongdong Li, Zeran Jia, Wenhao Zhang, Yuling Chen, Ruixue Zhao, Yan-Ping Zhang, Wen-Hong Zhang, Haiteng Deng, Yinqing Li, Wei Li, Shouhong Guang, Guangshuo Ou(*) (2023) Global histone H2B degradation regulates insulin/IGF signaling-mediated nutrient stress. The EMBO Journal (2023a) Aug 29:e113328. doi: 10.15252/embj.2022113328.
[8]Demin Xu(#), Xiangyang Chen(#), Yan Kuang, Minjie Hong, Ting Xu, Ke Wang, Xinya Huang, Chuanhai Fu, Ke Ruan, Chengming Zhu(*), Xuezhu Feng(*) and Shouhong Guang(*) (2023) rRNA intermediates coordinate the formation of nucleolar vacuoles in C. elegans. Cell Reports, 2023 Aug 1;42(8):112915. doi: 10.1016/j.celrep.2023.112915.
[9]Xinhao Hou(#), Mingjing Xu(#), Chengming Zhu(#), Jianing Gao, Meili Li, Xiangyang Chen, Cheng Sun, Björn Nashan, Jianye Zang, Ying Zhou(*), Shouhong Guang(*), and Xuezhu Feng(*) (2022) Systematic characterization of chromodomain proteins reveals an H3K9me1/2 reader regulating aging in C. elegans. Nature Communications, 2023 Mar 6;14(1):1254. doi: 10.1038/s41467-023-36898-y.
[10]Ting Xu,Shimiao Liao , Meng Huang, Chengming Zhu, Xiaona Huang, Qile Jin, Demin Xu, Chuanhai Fu, Xiangyang Chen(*), Xuezhu Feng(*) and Shouhong Guang(*) (2023) A ZTF-7/RPS-2 complex mediates the cold-warm response in C. elegans. PLoS Genetics, 2023 Feb 10;19(2):e1010628. doi: 10.1371/journal.pgen.1010628
[11]Meng Huang(#), Minjie Hong(#), Chengming Zhu, Di Chen(*), Xiangyang Chen(*), Shouhong Guang(*), and Xuezhu Feng(*) (2022) H3K9me1/2 methylation limits the lifespan of daf-2 mutants in C. elegans. Elife. 2022 Sep 20;11:e74812. doi: 10.7554/eLife.74812.
[12]Xuelian Ma(#), Shumin Cheng(#), Ruofan Ding, Zhaozhao Zhao, XuDong Zou, Shouhong Guang, Qixuan Wang, Huan Jing, Chen Yu, Ting Ni, Lei Li(*) (2022) ipaQTL-atlas: an atlas of intronic polyadenylation quantitative trait loci across human tissues. Nucleic Acids Research, 2022 Aug 31, https://doi.org/10.1093/nar/gkac736
[13]Xinhao Hou(#), Chengming Zhu, Mingjing Xu, Xiangyang Chen, Cheng Sun, Björn Nashana(*), Shouhong Guang(*), and Xuezhu Feng(*) (2022) The SNAPc complex mediates starvation-induced trans-splicing in C. elegans. Journal of Genetics and Genomics, 2022 Mar 10:S1673-8527(22)00076-5. doi: 10.1016/j.jgg.2022.02.024.
[14]Xiaoyang Wang(#), Chenming Zeng(#), Shanhui Liao(#), Zhongliang Zhu, Jiahai Zhang, Xiaoming Tu, Xuebiao Yao, Xuezhu Feng(*), Shouhong Guang(*), and Chao Xu(*) (2021) Molecular basis for PICS-mediated piRNA biogenesis and cell division. Nature Communications, 12, Article number: 5595 (2021) https://doi.org/10.1038/s41467-021-25896-7
[15]Zheng Xu(#), Jie Zhao, Minjie Hong, Chenming Zeng, Shouhong Guang(*), Yunyu Shi(*) (2021)Structural recognition of the mRNA 3’ UTR by PUF-8 restricts the lifespan of C. elegans. Nucleic Acids Research, Sept 3, 2021 https://doi.org/10.1093/nar/gkab754
[16]Shimiao Liao(#), Xiangyang Chen(#), Ting Xu(#), Qile Jin, Zongxiu Xu, Demin Xu, Xufei Zhou, Chengming Zhu(*), Shouhong Guang(*) and Xuezhu Feng(*) (2021)Antisense ribosomal siRNAs inhibit RNA polymerase I-directed transcription in C. elegans Nucleic Acids Research Aug 7, 2021 https://doi.org/10.1093/nar/gkab662
[17]Xinya Huang(#), Peng Cheng(#), Chenchun Weng, Zongxiu Xu, Chenming Zeng, Xiangyang Chen(*), Chengming Zhu(*), Shouhong Guang(*), and Xuezhu Feng(*) (2021) A chromodomain protein mediates heterochromatin-directed piRNA expression. PNAS, July 6, 2021 118 (27) e2103723118; https://doi.org/10.1073/pnas.2103723118
[18]Chenming Zeng (#), Chenchun Weng (#), Xiaoyang Wang (#), Yong-Hong Yan (#), Wen-Jun Li, Demin Xu, Minjie Hong, Shanhui Liao, Meng-Qiu Dong, Xuezhu Feng (*), Chao Xu (*), and Shouhong Guang (*) (2019) Functional proteomics identifies a PICS complex required for piRNA maturation and chromosome segregation. Cell Reports Volume 27, ISSUE 12, P3561-3572.e3, June 18, 2019, DOI: https://doi.org/10.1016/j.celrep.2019.05.076
[19]Qi Yan (#), Chengming Zhu (#), Shouhong Guang (*) and Xuezhu Feng (*) (2019) The Functions of Non-coding RNAs in rRNA Regulation. Frontiers in Genetics April 05; Vol. 10, doi: 10.3389/fgene.2019.00290
[20]Chenchun Weng (#), Joanna Kosalka (#), Ahmet C. Berkyurek (#), Przemyslaw Stempor, Xuezhu Feng, Hui Mao, Chenming Zeng, Wen-Jun Li, Yong-Hong Yan, Meng-Qiu Dong, Natalia Rosalía Morero, Cecilia Zuliani, Orsolya Barabas, Julie Ahringer, Shouhong Guang (*), and Eric A. Miska (*) (2018) The USTC complex co-opts an ancient machinery to drive piRNA transcription in C. elegans. Genes & Development, 2019, 33(1-2): 90-102.
[21]Chengming Zhu (#), Qi Yan (#), Chenchun Weng , Xinhao Hou , Hui Mao , Dun Liu , Xuezhu Feng (*) , Shouhong Guang (*) (2018) Erroneous ribosomal RNAs promote the generation of antisense ribosomal siRNA. Proceedings of the National Academy of Sciences, 2018, 115(40): 10082-10087.. doi: 10.1073/pnas.1800974115.
[22]Fei Xu (#), Xuezhu Feng (#), Xiangyang Chen, Chenchun Weng, Qi Yan, Ting Xu, Minjie Hong, and Shouhong Guang (*)(2018)A cytoplasmic Argonaute protein promotes the inheritance of RNAi. Cell Reports, 2018, 23(8): 2482-2494.
[23]Chen X (#*), Liao S (#), Huang X, Xu T, Feng X, Guang S (*). (2018) Targeted Chromosomal Rearrangements via a Combinatorial Use of CRISPR/Cas9 and Cre/LoxP Technologies in Caenorhabditis elegans. Genes Genomes Genetics, 2018, 8(8): 2697-2707. doi: 10.1534/g3.118.200473.
[24]Fei Xu (#), Shouhong Guang (*), and Xuezhu Feng (*) (2018) Distinct nuclear and cytoplasmic machineries cooperatively promote the inheritance of RNAi in C. elegans. Biology of the Cell 2018 Aug 22. doi: 10.1111/boc.201800031 (review)
[25]Xufei Zhou (#), Xuezhu Feng (#), Hui Mao, Mu Li, Fei Xu, Kai Hu, and Shouhong Guang(*) (2017) RdRP-synthesized antisense ribosomal siRNAs silence pre-rRNA via the nuclear RNAi pathway. Nature Structural & Molecular Biology 2017 Mar;24(3):258-269. doi: 10.1038/nsmb.3376.
[26]Zhou X, Chen X, Wang Y, Feng X, Guang S. (2017) A new layer of rRNA regulation by small interference RNAs and the nuclear RNAi pathway. RNA Biol. 2017 Jun 22:0. doi: 10.1080/15476286.2017.1341034. (review)
[27]Li, Gaopeng; Wu, Xiaoli; Qian, Wenchang; Cai, Huayong; Sun, Xinbao; Zhang, Weijie; Tan, Sheng; Wu, Zhengsheng; Qian, Pengxu; Ding, Keshuo; Lu, Xuefei; Zhang, Xiao; Yan, Hong; Song, Haifeng; Guang, Shouhong; Wu, Qingfa; Lobie, Peter E.; Shan, Ge; Zhu, Tao*.CCAR1 5' UTR as a natural miRancer of miR-1254 overrides tamoxifen resistance.Cell Research, 2016, 26(6): 655-673. doi: 10.1038/cr.2016.32.
[28]Xiangyang Chen, Xuezhu Feng (*) and Shouhong Guang (*) (2016) Targeted genome engineering in Caenorhabditis elegans. Cell & Bioscience 2016 6:60, DOI: 10.1186/s13578-016-0125-3 (review)
[28]Mao, Hui; Zhu, Chengming; Zong, Dandan; Weng, Chenchun; Yang, Xiangwei; Huang, Hui; Liu, Dun; Feng, Xuezhu*; Guang, Shouhong*.The Nrde Pathway Mediates Small-RNA-Directed Histone H3 Lysine 27 Trimethylation in Caenorhabditis elegans.Current Biology, 2015, 25(18): 2398-2403.
[28] Chen, Xiangyang; Li, Mu; Feng, Xuezhu*; Guang, Shouhong*. (2015) Targeted Chromosomal Translocations and Essential Gene Knockout Using CRISPR/Cas9 Technology in Caenorhabditis elegans. Genetics 2015 Dec;201(4):1295-306 doi: 10.1534/genetics.115.181883.
[29]Zhou X (#), Xu F (#), Mao H, Ji J, Yin M, Feng X (*), and Shouhong Guang (*) (2014) Nuclear RNAi Contributes to the Silencing of Off-Target Genes and Repetitive Sequences in Caenorhabditis elegans. Genetics 2014 May;197(1):121-132.
[30]Xiangyang Chen (#), Fei Xu (#), Chengming Zhu, Jiaojiao Ji, Xufei Zhou, Xuezhu Feng (*), and Shouhong Guang (*) (2014) Dual sgRNA-directed gene knockout using CRISPR/Cas9 technology in Caenorhabditis elegans. Scientific Reports 2014 Dec. 22;4:7581.
[31]Mao, Hui; Feng, Xue-zhu; Guang, Shou-hong*.Treating liver cancer with antibiotics?Acta Pharmacologica Sinica, 2013, 34(8): 989-990.; doi: 10.1038/aps.2013.102.
[32]Xuezhu Feng and Shouhong Guang(*).Small RNAs, RNAi and the inheritance of gene silencing in Caenorhabditis elegans.Journal of Genetics and Genomics, 2013, 40(4): 153-160.
[33]Xuezhu Feng and Shouhong Guang(*).Non-coding RNAs mediate the rearrangements of genomic DNA in ciliates.Science China Life Sciences, 2013, 56(10): 937-943.
[34]Ge Shan*; shouhong guang*.chinese worm community made delightly wiggles in Hefei September 6 to September 8, 2013。Science China Life Sciences, 2013, 56(11): 1066-1066.
[35]Sam Guoping Gu; Julia Pak; Shouhong Guang; Jay M. Maniar; Scott Kennedy; Andrew Fire*.Amplification of siRNA in Caenorhabditis elegans generates a transgenerational sequence-targeted histone H3 lysine 9 methylation footprint.Nature Genetics, 2012, 44(2): 157-164.
[36]Burkhart, Kirk B; Guang, Shouhong; Buckley, Bethany A; Wong, Lily; Bochner, Aaron F; Kennedy, Scott*.A pre-mRNA-associating factor links endogenous siRNAs to chromatin regulation.PLoS Genetics, 2011, 7(8):e1002249
[37]Shouhong Guang; Aaron F. Bochner; Kirk B. Burkhart; Nick Burton; Derek M. Pavelec; Scott Kennedy*.Small regulatory RNAs inhibit RNA polymerase II during the elongation phase of transcription.Nature, 2010, 465(7301): 1097-1101.
[38]Shouhong Guang; Aaron F. Bochner; Derek M. Pavelec; Kirk B. Burkhart; Sandra Harding; Jennifer Lachowiec; Scott Kennedy*.An Argonaute transports siRNAs from the cytoplasm to the nucleus.Science, 2008, 321(5888): 537-541.
[39]Shouhong Guang; Alicia M. Felthauser; Janet E. Mertz*.Binding of hnRNP L to the pre-mRNA processing enhancer of the herpes simplex virus thymidine kinase gene enhances both polyadenylation and nucleocytoplasmic export of intronless mRNAs.Molecular and Cellular Biology, 2005, 25(15): 6303-6313.
[40]Shouhong Guang; Mertz, J.E.*.Pre-mRNA processing enhancer (PPE) elements from intronless genes play additional roles in mRNA biogenesis than do ones from intron-containing genes.Nucleic Acids Research, 2005, 33(7): 2215-2226.
[41]Zeng, W., Zhang, X., Tu, X., Guang, S., Xiao, Y., and Shi, Y. (2001) Expression and purification of the DNA-binding domain of the human transcription factor E2F1. Protein Expr. Purif. 21(1):99-104.
[42]Xia, Y.L., Wu, J.H., Guang, S., and Shi, Y. (2000) Proton NMR investigation of heme and surrounding proton in low-spin cyanide-ligated bacterial hemoglobin from vitreoscilla. Sci. China Ser (China). C 43(1):57-67.
[43]Xia, Y.L., Wu, J.H., Guang, S., and Shi, Y. (1998) The application of nuclear magnetic resonance in paramagnetic metallic protein - a vitreoscilla hemoglobin. Acta Biophysica Sinica (China) 14(3):392-400.
[44]Guang, S., Wu, J.H., Yu, T., Xia, Y.L., and Shi, Y. (1998) Solution structure of a fragment of the dimerization domain of DP-1 determined by 1H-nuclear magnetic resonance and distance geometry. Biochim. Biophys. Acta - Protein Structure and Molecular Enzymology 1429(1):18-28.
[45]Guang, S., Wu, J.H., Tao, L., Xia, Y.L., and Shi, Y. (1998) Solution structure of a fragment of the dimerization domain of E2F-1 determined by circular dichroism, 1H-nuclear magnetic resonance and distance geometry. Biochim. Biophys. Acta - Protein Structure and Molecular Enzymology 1388(1):111-122.
[46] Xiangyang Chen, Shouhong Guang, (2021) Genome manipulation using CRISPR/Cas9 technology in C. elegans, The 6th Chinese C. elegans Meeting, Workshop, Oct 17
中文期刊论文:
[1]徐飞, 冯雪竹, Xiangyang Chen, Chenchun Weng, Qi Yan, Ting Xu, Minjie Hong, 光寿红. 一个细胞质Argonaute蛋白介导RNA干扰的遗传[J]. 科学新闻, 2019, (02): 128.
[2]陈向阳, 冯雪竹, 光寿红*. 靶向基因编辑技术在秀丽隐杆线虫中的应用[J]. 中国科学:生命科学, 2018, 48 (03): 266-277.
[3]冯雪竹, 光寿红. 细胞核内小干扰RNA介导的表观遗传和基因表达调控[J]. 中国科学:生命科学, 2017, 47 (01): 59-68.
[4]Hui Mao, Chengming Zhu, Dandan Zong, Chenchun Weng, Xiangwei Yang, Hui Huang, Dun Liu, 冯雪竹, 光寿红. 秀丽线虫中小RNA通过细胞核RNA干扰通路介导组蛋白3赖氨酸27的三甲基化[J]. 科学新闻, 2016, (01): 109.
[5]冯雪竹, 光寿红. 秀丽线虫细胞核内小干扰RNA调控基因表达的机制研究[J]. 中国科学技术大学学报,2013, 43(11)100-105
[6]夏佑林,吴季辉,光寿红,张海阳,梁山,施蕴渝. Proton NMR investigation of heme and surrounding proton in low-spin cyanide-ligated bacterial hemoglobin from Vitreoscilla[J]. Science in China(Series C:Life Sciences), 2000, (01): 57-67.
[7]夏佑林,吴季辉,光寿红,刘琴,张海阳,梁山,施蕴渝. 低自旋氰配位紫色震颤菌血红蛋白血红素及其周围质子的核磁共振研究[J]. 中国科学C辑:生命科学, 1999, (05): 475-483.
[8]夏佑林,吴季辉,光寿红,刘琴,张海阳,粱山,施蕴渝. 核磁共振波谱方法在顺磁金属蛋白-紫色震颤菌血红蛋白中的应用[J]. 生物物理学报, 1998, (03): 11-20.
[9]Farees ud din mufti & 光寿红. (2016). Erroneous transcript can trigger generation of siRNA by recruiting RdRP in Caenorhabditis elegans. (eds.) 第九届全国核糖核酸学术讨论会论文集 (pp.23).
荣誉奖励:
1.中组部青年**计划”入选者。
2.中国科学院“**计划”入选者。
3.获中国科学院院长奖及美国心脏协会博士后奖。
学术交流:
主持过第三届全国线虫大会以及第八届全国核糖核酸会议,也参加了全国非编码核糖核酸的香山会议。
资料更新中……
中国科技大学Cell子刊发表RNA研究新成果
生物体内存在大量不编码蛋白质的非编码RNA,它们广泛参与了关键性细胞功能的调控。近年来人们发现,非编码RNA出现异常与许多重要的疾病有关,了解这些RNA有助于更好的理解和治疗相关疾病。
小干扰RNA(siRNA)是一种广为人知的非编码RNA,能够调控细胞核中的基因表达。siRNA介导的染色质修饰已经在植物和酵母中被广泛研究,但科学家们对动物的这种染色质修饰还不够了解。
中国科学技术大学的研究人员日前发现,Nrde(nuclear RNAi defective)通路介导了siRNA诱导的组蛋白甲基化。这一成果发表在九月十日的Current Biology杂志上,文章的通讯作者是中国科技大学的光寿红(Shouhong Guang)教授和冯雪竹(Xuezhu Feng)博士。
线虫的Nrde(nuclear RNAi defective)通路可以将siRNA从细胞质转运到细胞核、调控转录延伸、诱导H3K9三甲基化和介导RNAi的跨代遗传。研究人员发现,结合NRDE的内源22G RNA和外源RNAi都能通过Nrde通路诱导序列特异性的H3K27三甲基化,而且这种H3K27me3状态可以遗传好几代。
此外,piRNA和WAGO-1相关的siRNA也能诱导H3K27甲基化。有趣的是CSR-1相关的内源siRNA不能触发H3K27甲基化,但外源dsRNA能够通过Nrde通路在CSR-1靶位点诱导H3K27甲基化。
进一步研究表明,H3K27三甲基化和H3K9三甲基化的遗传学要求并不相同,K27甲基化需要mes-2,而K9甲基化需要set-25和met-2。去除mes-2会使细胞核出现RNAi缺陷。这些结果说明,在线虫中dsRNA触发的染色质修饰,是一种涉及Nrde通路的序列特异性应答。
作者简介:
光寿红 1996年在中国科学技术大学生物系获得学士学位,1996-1999年师从中国科大施蕴渝院士进行多肽的溶液构象研究,并获得硕士学位。1999-2004年,在美国威斯康星大学癌症研究所师从Janet Mertz教授,研究真核生物中病毒起源的无内含子RNA的表达和调控机制,并获得博士学位。2005-2010年,作为博士后在威斯康星大学遗传系Scott Kennedy助理教授实验室,从事模式生物中小干扰RNA的功能和调控机理的研究。进一步研究小干扰RNA的功能和调控机制。在包括Nature和Science在内的国际著名期刊上发表论文12篇(其中第一作者6篇),2篇论文被Faculty of 1000 Biology收录并给予高度评价,曾获得中国科学院院长奖及美国心脏协会博士后奖。中组部青年**计划”入选者。
来源: 生物通 2015-9-15
中国科技创新人物云平台暨“互联网+”科技创新人物开放共享平台(简称:中国科技创新人物云平台)免责声明:
1、中国科技创新人物云平台是:“互联网+科技创新人物”的大型云平台,平台主要发挥互联网在生产要素配置中的优化和集成作用,将互联网与科技创新人物的创新成果深度融合于经济社会各领域之中,提升实体经济的创新力和生产力,形成更广泛的以互联网为基础设施和实现工具的经济发展新形态,实现融合创新,为大众创业,万众创新提供智力支持,为产业智能化提供支撑,加快形成经济发展新动能,促进国民经济提质增效升级。
2、中国科技创新人物云平台暨“互联网+”科技创新人物开放共享平台内容来源于互联网,信息都是采用计算机手段与相关数据库信息自动匹配提取数据生成,并不意味着赞同其观点或证实其内容的真实性,如果发现信息存在错误或者偏差,欢迎随时与我们联系,以便进行更新完善。
3、如果您认为本词条还有待完善,请编辑词条。
4、如果发现中国科技创新人物云平台提供的内容有误或转载稿涉及版权等问题,请及时向本站反馈,网站编辑部邮箱:kjcxac@126.com。
5、中国科技创新人物云平台建设中尽最大努力保证数据的真实可靠,但由于一些信息难于确认不可避免产生错误。因此,平台信息仅供参考,对于使用平台信息而引起的任何争议,平台概不承担任何责任。

















